导语
2015年7月5日上午,2015华东肿瘤论坛在上海吴孟超肿瘤医学中心-宁波第五医院•宁波肿瘤医院顺利召开。本次会议围绕“大数据时代肿瘤个体化医疗的精准决策”主题展开。来自上海市肺部肿瘤临床医学中心的陆舜教授做了题为“驱动基因指导下的肺癌靶向治疗进展”的报告。报告围绕过去50年肺癌治疗的进展、肺癌个体化治疗的现状和未来个体化治疗的发展方向三个话题进行了十分精彩的阐述。医脉通将报告内容总结如下:

陆舜教授
过去50年肺癌治疗的进展
Nature Reviews Clinical Oncology 5月份发表了一篇文章总结了过去50年肺癌治疗的演变。上世纪70年代初期,人们才开始探索将化疗应用于肺癌治疗。这是由于在此之前的化疗药物对肺癌没有效果。大概在1994年,FDA才首次批准肺癌为含铂两药治疗方案的适应症。1995年~2000年,含铂两药方案在肺癌治疗的领域里进行了广泛的应用。2002年发表在NEJM上的研究表明各种含铂两药方案比较,疗效是没有差异的,差异仅在于毒性和耐受性。
本世纪初,一代酪氨酸激酶抑制剂(TKI),被广泛使用之后,人们才首次在肺癌中发现了第一个驱动基因。而在这个过程中,更重要的是检测手段的演变。从最开始的免疫组化,到后来BR 21研究认为荧光原位杂交技术(FISH)检测很重要。而到了2009年,IPASS的研究则指出FISH检测并不重要,更重要的是突变检测。随着检测方法的发展,未来临床医生可能会面对各种的检测方法和大量的数据。面对这种情况,临床医生应该更加关注哪种检测方法是有效的、标准化的。例如现在检测EGFR,标准化的方法是应用Scorpions ARMS检测,而不是直接测序法,因为直接测序法敏感性不够。
2007年,EML4-ALK融合基因在NSCLC中被首次发现,这在肺癌的研究中是非常成功的。因为在此之前,人体内很少发现染色体重排现象,只有在白血病中发现过费城染色体。ALK基因发现之后很快就被转化成药物,2011年,FDA就批准克唑替尼用于ALK基因阳性的NSCLC治疗。
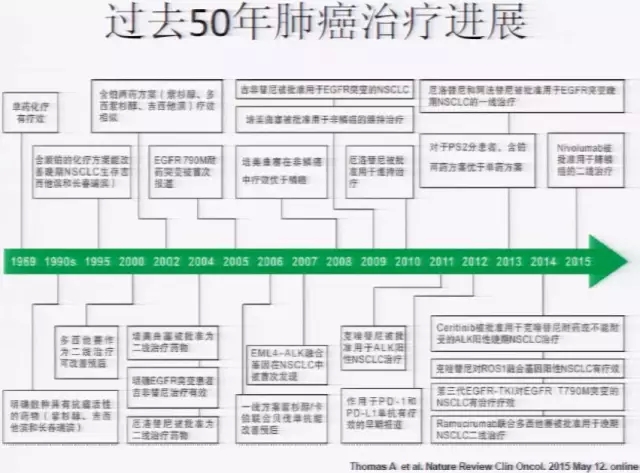
到了2010年之后,人们发现了更多的位点。自此肺癌的个体化治疗才开始发展起来,才有了现在驱动基因指导下的个体化治疗,和未来的精准医疗在肺癌上的应用。借用Collins在ASCO大会上的阐述,“我们要改变我们的医疗模式,从针对特定器官的治疗转变为针对特定分子靶点的治疗。”在未来,临床医生很可能由基于外科学器官概念的分类转变为基于分子位点治疗的分类。
肺癌个体化治疗的现状
•何为驱动基因
对于科学研究来讲,当一个基因突变(过表达/扩增)能够对肿瘤的发生、发展、侵犯和转移起控制作用,并且抑制这个基因表达的蛋白或基因通路可以中止肿瘤发展的相关事件时,这个基因就可以被称为驱动基因。但是对于临床医生来讲,更重要的是针对驱动基因的治疗可以达到50%以上的缓解率和6个月以上的PFS时,这个驱动基因才可以算有意义。否则可能没有临床意义。
•NSCLC分子靶向治疗
近两年,随着驱动基因不断被发现,人们对肺癌的驱动基因了解也愈发深入。不同的驱动基因突变率不同,治疗效果、药物反应和预后都不同。甚至最近发现,同一种药物对同一个驱动基因的不同位点上发生的突变都有不同的疗效。而且,当一种药出现耐药性后,就会出现新药抵抗耐药性,而新药很快又被发现有新的耐药性。现在“肺癌不是一种病,而是很大的一组病”。因此现在临床医生最迫切的需求是针对不同的驱动基因,找到有效的、易于检测的生物标志物(biomarker)。
成药性驱动基因(Drugable driver gene)是最近提出的概念,指的是已经有药物可以治疗的驱动基因。关于这一点需要注意的是,同一个驱动基因突变造成的不同疾病,应用同一种药物时使用剂量也有可能不同。例如,达沙替尼治疗DDR2突变的白血病患者时使用的推荐剂量应用于治疗DDR2突变的肺鳞癌患者就会产生较大的药物毒性,这是由于患者群体不同,药代动力学的情况也不同。因此在精准医疗时代,在数据的解读和利用时,临床医生需要谨慎。
•个体化治疗的进展
由于亚裔肺腺癌患者EGFR突变率较高,个体化治疗在亚裔肺腺癌患者取得了较好的成果。去年关于阿法替尼与化疗的治疗效果比较的研究发现,阿法替尼治疗EXON 19突变的患者的总生存要好于化疗,而对于EXON 21突变的患者,单纯讲疗效不考虑生活质量的话,是没有统计学差异的。
针对EGFR的三代TKI药物现在已进入三期临床阶段。在晚期初治EGFR敏感突变人群中,三代TKI的代表AZD9291显示了良好的疗效和可管理的耐受性。一、二、三代TKI相比较,二代TKI的优势在于对于野生型EGFR患者,二代TKI也有较好的治疗效果。而三代TKI的优势则在于其对耐药突变T790M患者有很好的疗效。二代与一代、三代与一代的头对头的临床试验正在进行,结果值得期待。
去年,美国和日本相继批准二代ALK抑制剂进入临床,而针对cMET、ROS1、BRAFV600E的药物疗效也得到了证实。
关于肿瘤精准治疗还有一点需要注意:临床治疗与科研不同,治疗方法需要通过食品药品监督管理局的验证与审批才可以广泛应用于临床。
近年来关于耐药性研究的进展也非常快,不同药物的耐药机制是相似的。对于EGFR耐药的发现用了3年的时间,对于ALK,随机三期临床试验是与耐药性同时发表的,而ROS1的临床试验进行的同时就发表了耐药性的研究,AZD 9291甚至还在早期临床试验阶段就已经有耐药性的研究发表了。
未来晚期肺癌个体化治疗

活检——治疗——耐药——再活检——再治疗
Nature Reviews Clinical Oncology的总编曾说,“战胜肿瘤就要像肿瘤一样思考”。未来二代基因测序技术毫无疑问将会成为重要的检测手段,但是更重要的是不断进行活检,找到耐药,然后治疗。这个过程会改变整个临床诊疗模式和个体化治疗模式。而针对驱动基因治疗的发展可能很快就会达到瓶颈期,也许未来“精准免疫治疗”能够获得突破,从而实现肺癌患者OS超过5年,成为慢性疾病的目标。
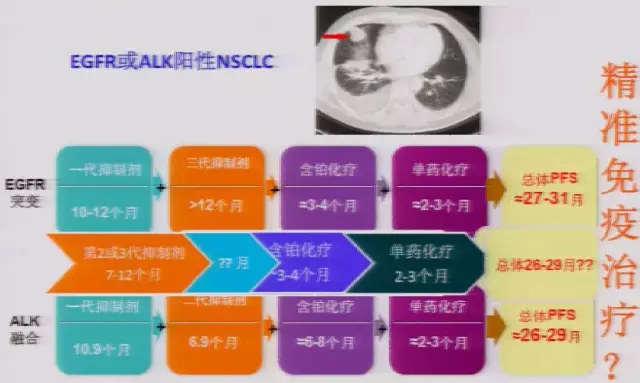
精准免疫治疗或成为突破点
(文章来源于《医脉通肿瘤科》)
