医脉通整理,未经授权,不可转载。
2017年7月7日,由中国临床肿瘤学会(CSCO)携手美国临床肿瘤学会(ASCO)于“临床肿瘤学新进展学术研讨会――(Best of ASCO® Event in China)于上海富悦大酒店召开。8日下午,江泽飞教授对ASCO2017后,乳腺癌年度临床研究进展和对临床工作带来的启示进行了大盘点和精彩点评,以下是详细内容。

江泽飞教授指出,随着乳腺癌精准治疗时代来临,应该在精准指导下对乳腺癌进行个体化的分类治疗。各个干预手段的“加减法”为乳腺癌治疗领域本年度最为热议的话题。
减法

由于后续治疗手段越来越充分,所以对于手术来说应该适当的做出“减法”。
例如,更多的保乳术(BCT)代替了改良根治术(MRM),更多腋窝前哨淋巴结活检术(SLNB)代替了腋窝清扫术(ALND)。
放射治疗方面,靶区体积也在逐渐的缩小,有些患者可以行部分乳房照射(APBI),甚至可以豁免。
在精准时代中,辅助化疗方案也在一些患者中做出了“减法”,患者用药的周期数和个数都有做“减法”的尝试。

早期乳腺癌(EBC)的辅助化疗领域中,最早的标准为CMF×6方案;
随着蒽环类的加入,研究证实AC×4方案与CMF×6方案效果类似,其周期数较少,所以AC方案逐渐成为了首选;
紫杉类加入之后,研究证实AC×4→T×4要优于原有的AC方案,AC→T成为了标准治疗。
随后,AC→T的方案正在进行剂量密集方案的优化与探索。
加法
乳腺癌治疗的“加法”主要来源于精准治疗。
在内分泌治疗中,出现了CDK4/6抑制剂、mTOR抑制剂等与传统AI联合或互相联合的探索研究。

靶向治疗方面,也出现了一些双靶向药物联合治疗的临床研究。
乳腺癌的免疫治疗领域较其它癌种可能有一些落后,但是免疫治疗联合化疗或靶向药物,以及免疫治疗之间的联合可能会成为未来探索的方向。
强化辅助内分泌治疗
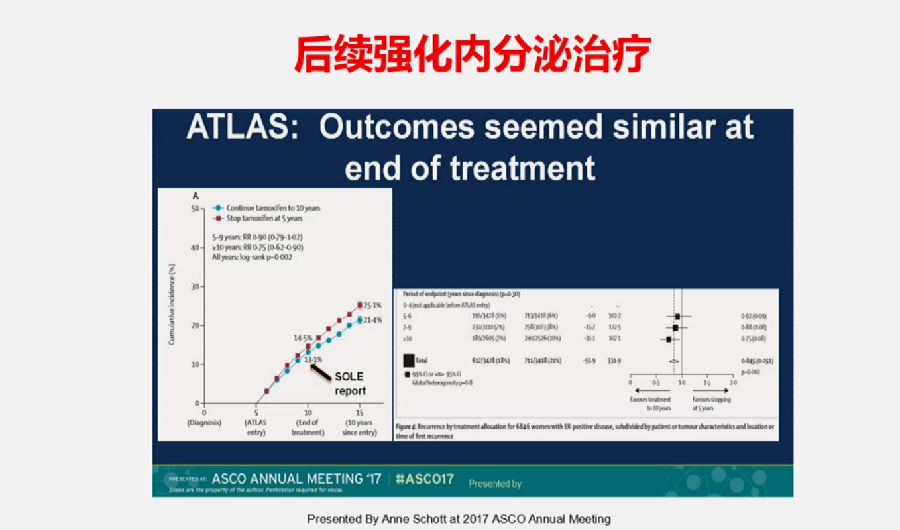
ATLAS研究结果表明,术后口服10年以上他莫昔芬(TAM)的患者复发风险小于口服5-9年的患者(RR: 0.90 vs 0.75, p=0.002)。标志着术后辅助后续强化内分泌治疗已经有了循证医学证据。
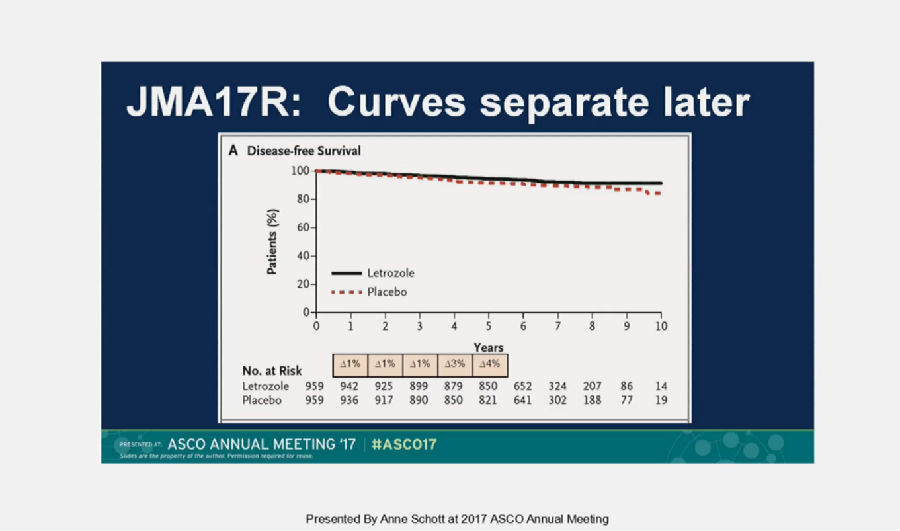
在JMA.17R研究的长期随访之后,口服芳香化酶抑制剂(AI)10年以上与5年AI相比,也得到了相似的结果。
克服内分泌耐药
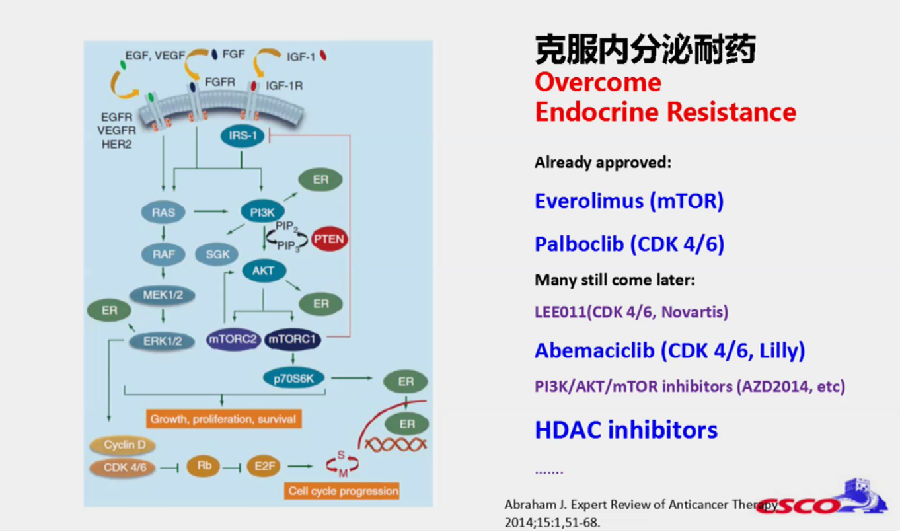
随着精准医学药物的研发,现在可以通过CDK4/6抑制剂、mTOR抑制剂、HDAC抑制剂等药物联合传统内分泌治疗药物,或者互相联合,达到克服内分泌耐药的目的。
这些“加法”的循证医学证据支持来源于很多的临床研究。
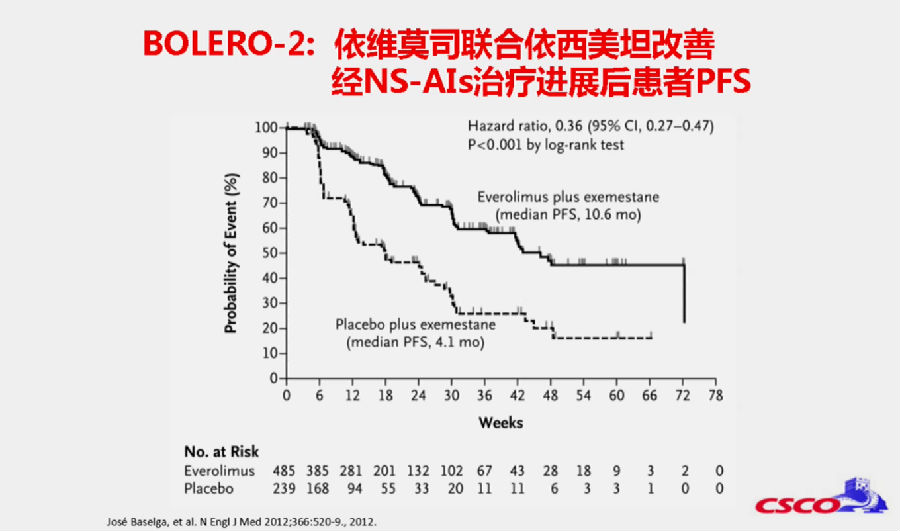
例如,在BOLERO-2研究中,依维莫司联合依西美坦明显改善了经过NS-AI治疗进展后患者的无进展生存期(PFS)(10.6个月 vs 4.1个月; HR, 0.36; 95%CI, 0.27-0.47; P<0.001)。
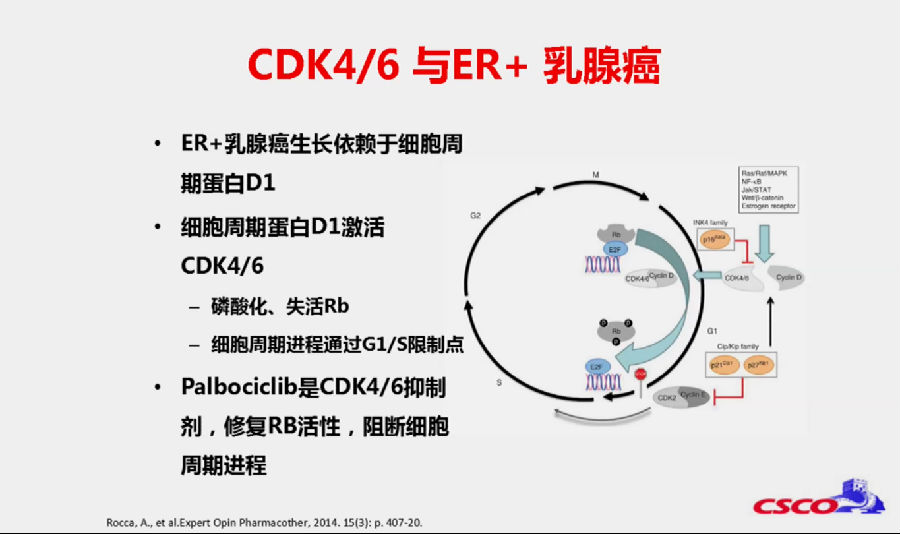
一系列CDK4/6抑制剂相关的临床研究也证实了针对该通路靶向药物的前景。由于内分泌治疗相对毒性较低,所以可以联合一种像CDK4/6抑制剂这样毒性稍高但是可以耐受的药物进行治疗。
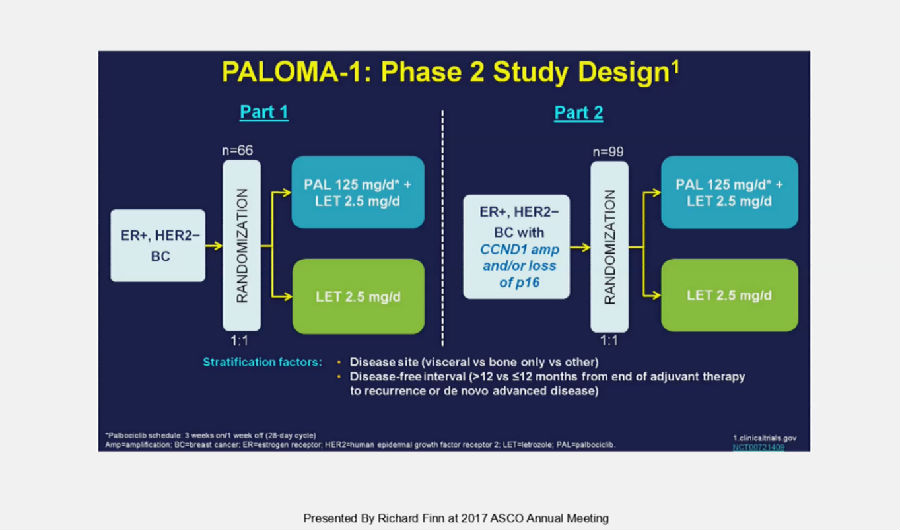
例如在今年ASCO上汇报的POLOMA-1 Ⅱ期临床研究,目的为探究在ER+,HER-2阴性的进展期乳腺癌一线治疗中,对比来曲唑+Palbociclib与来曲唑单药的有效性与安全性。
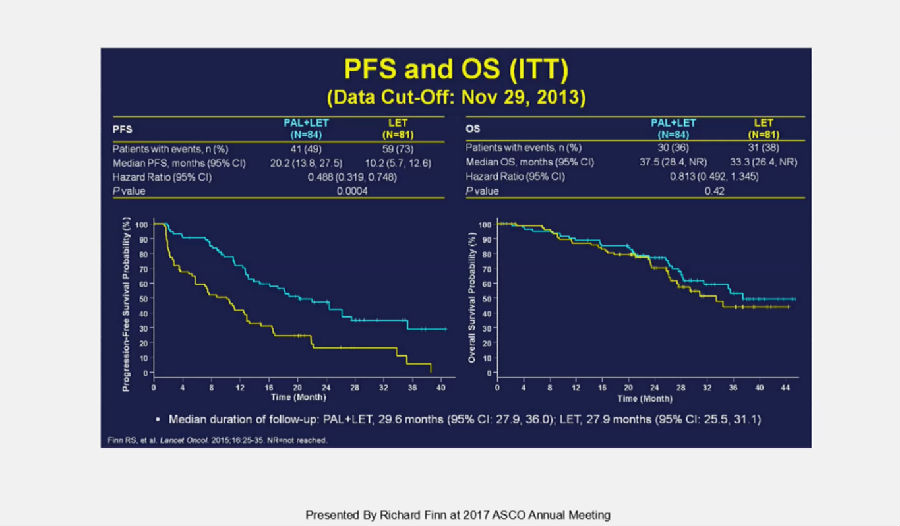
结果表明,联合组较单药组可显著延长患者的PFS(20.2个月 vs 10.2个月;HR, 0.488; 95%CI: 0.319,0.748; p<0.0004)。
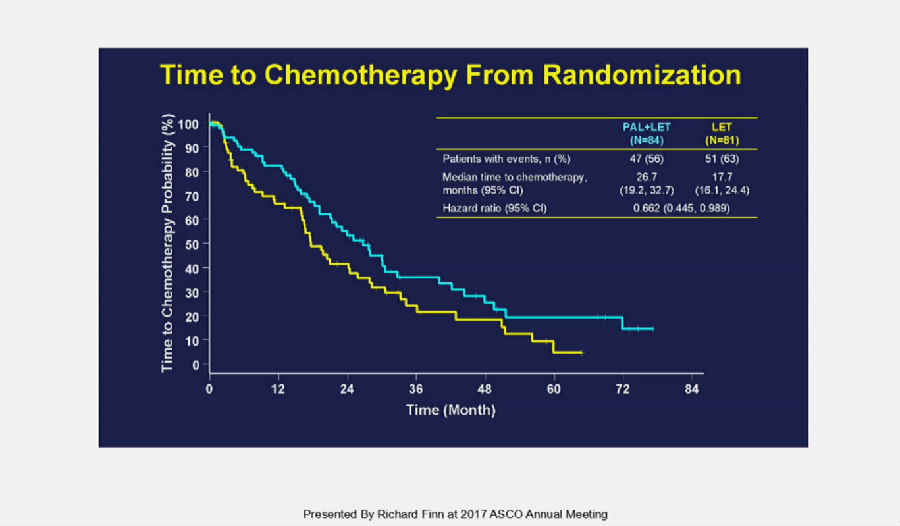
联合组与单药相比,从随机化至化疗的时间也明显延长(26.7个月 vs 17.7个月; HR, 0.662, 95%CI: 0.445, 0.989),联合用药可以让患者具有更多“Chemo Free”的时间,使患者获益。
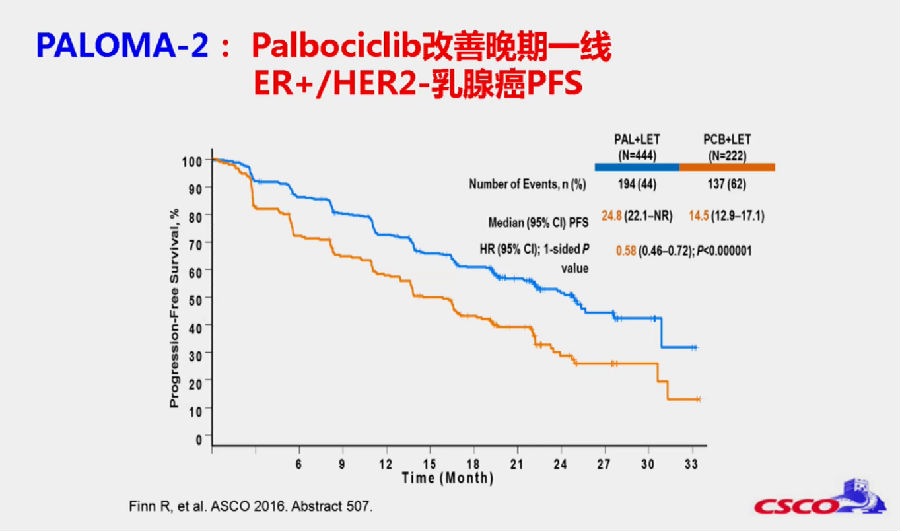
PALOMA-2研究也得到了类似的结果,palbociclib+来曲唑与单药来曲唑患者的PFS分别为24.8个月 vs 14.5个月(HR, 0.58; 95%CI: 0.46-0.72; p<0.000001)。
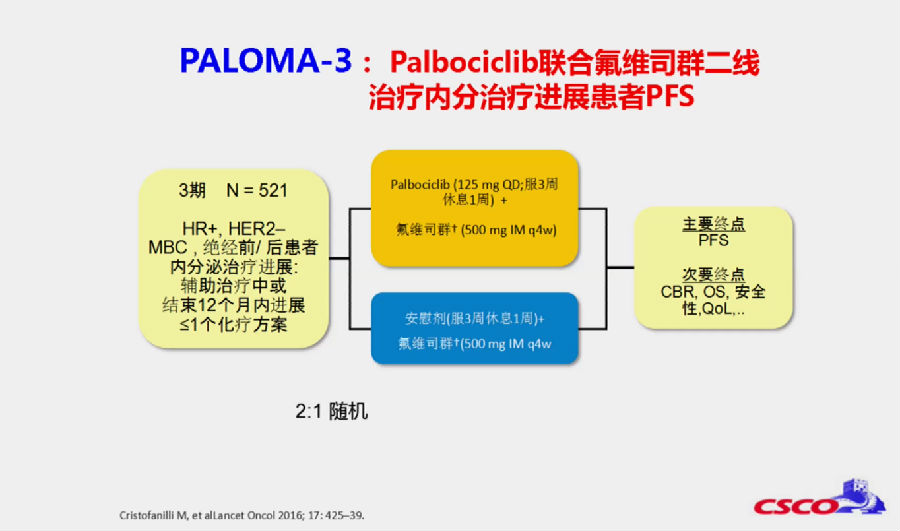
PALOMA-3目的是探究既往行一线内分泌治疗进展,以及辅助治疗中或结束12个月内进展的HR+/HER-2-的转移性乳腺癌(MBC)患者中,palbociclib联合氟维司群对比安慰剂+氟维司群的有效性与安全性。
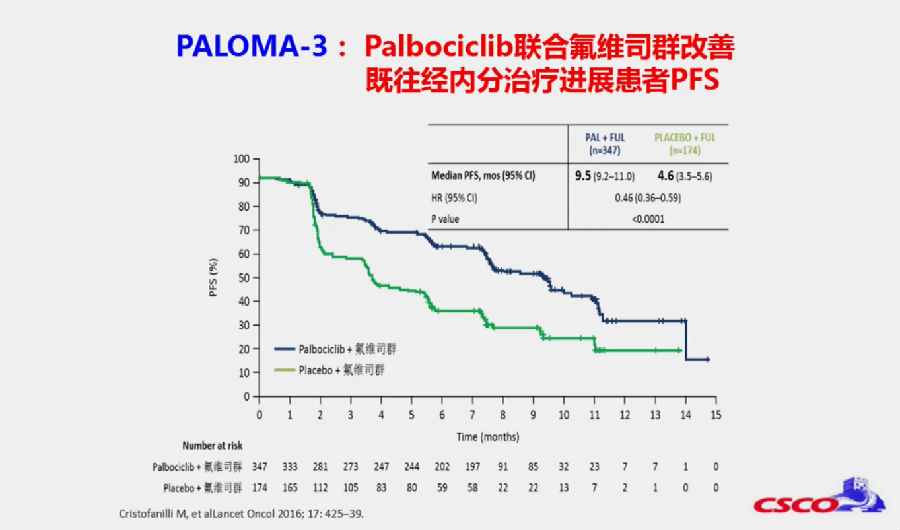
结果表明,联合组较对照组的PFS分别为9.5个月 vs 4.6个月(HR, 0.46; 95%CI: 0.36-0.59; p<0.0001)。
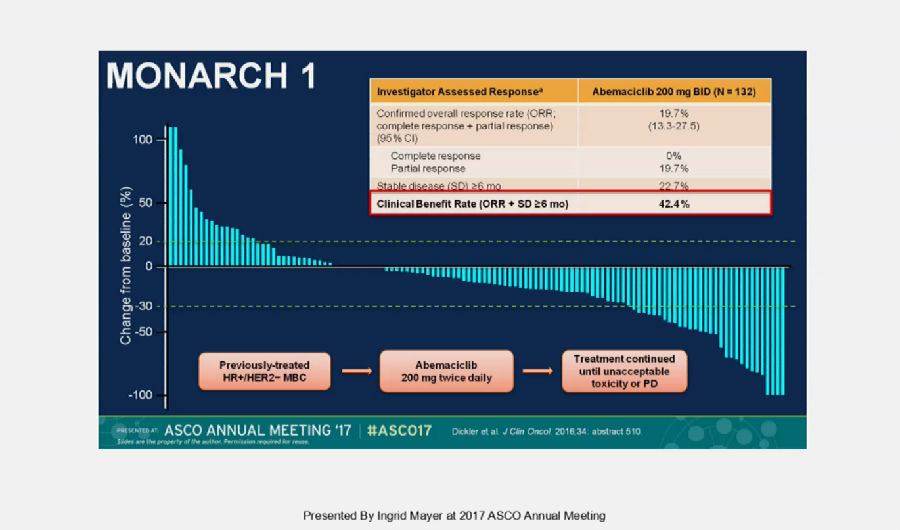
另外一种CDK4/6抑制剂abemaciclib的单药治疗也在既往接受过多线治疗的,HR+/HER-2-转移性乳腺癌中可以取得良好的效果,ORR可达42.4%。
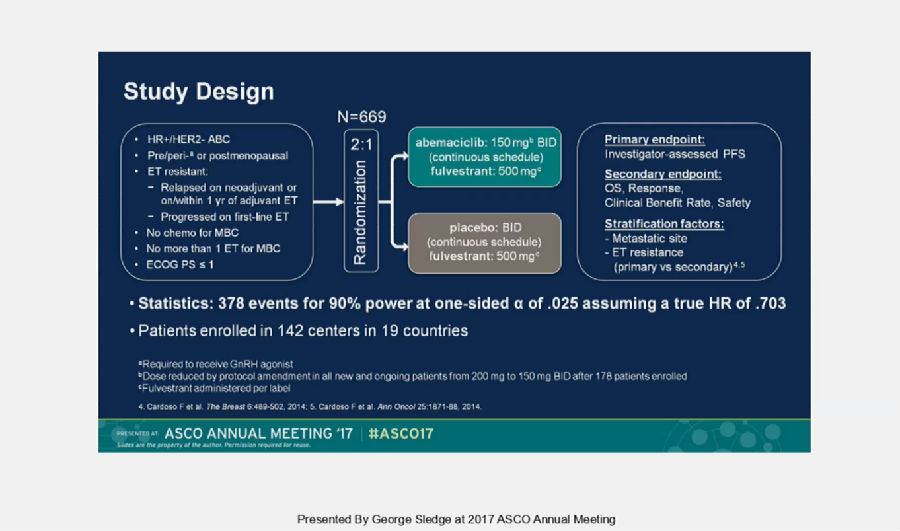
Monarch 2研究目的是探究在既往接受辅助/新辅助内分泌治疗或一线内分泌治疗进展,HR+/HER-2-的MBC中,abemaciclib联合氟维司群对比安慰剂联合氟维司群的有效性及安全性。
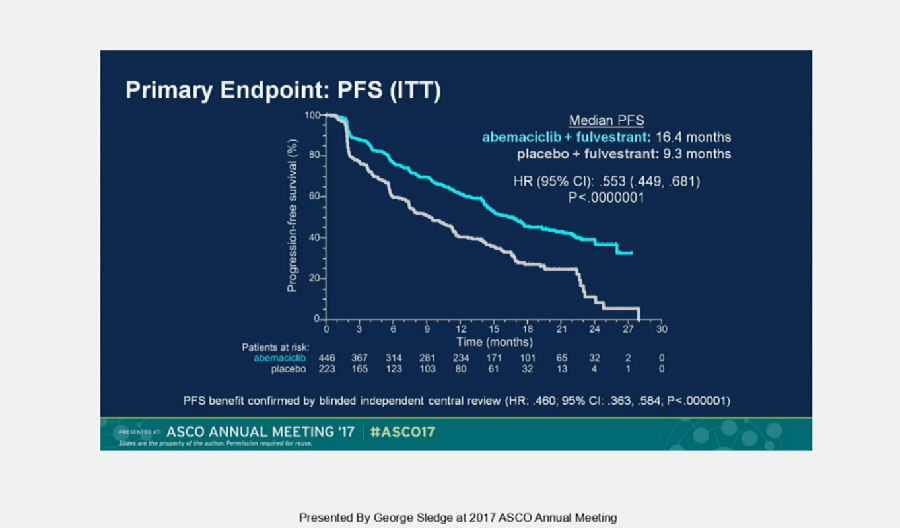
结果表明,治疗组与对照组的PFS分别为16.4个月和9.3个月(HR, 0.553; 95%CI: 0.449, 0.681; p<0.0000001)。
江泽飞教授表示,国内Abemaciclib联合氟维司群的研究也已经启动,希望能使更多的患者获益,并为中国患者提供更多的循证医学证据支持。
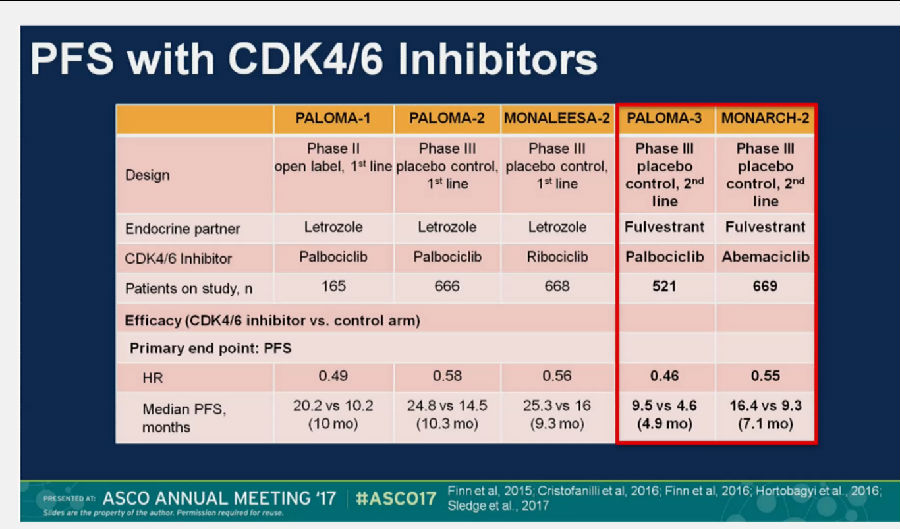
如果把CDK4/6抑制剂的相关研究汇总,可以看到在一线治疗中,CDK4/6抑制剂联合AI可以明显改善患者的PFS,所以单一使用传统AI的时代可能会慢慢的进入尾声。
而在既往接受过内分泌治疗患者的二线治疗来说,CDK4/6抑制剂联合氟维司群也能较氟维司群带来更多的PFS获益。
但是,不同干预手段带来的生存获益是有区别的。即使相同的对照组,在不同临床研究中的生存数据也不尽相同。这需要我们对临床研究设计的纳入人群进行深入分析,进行综合判断。
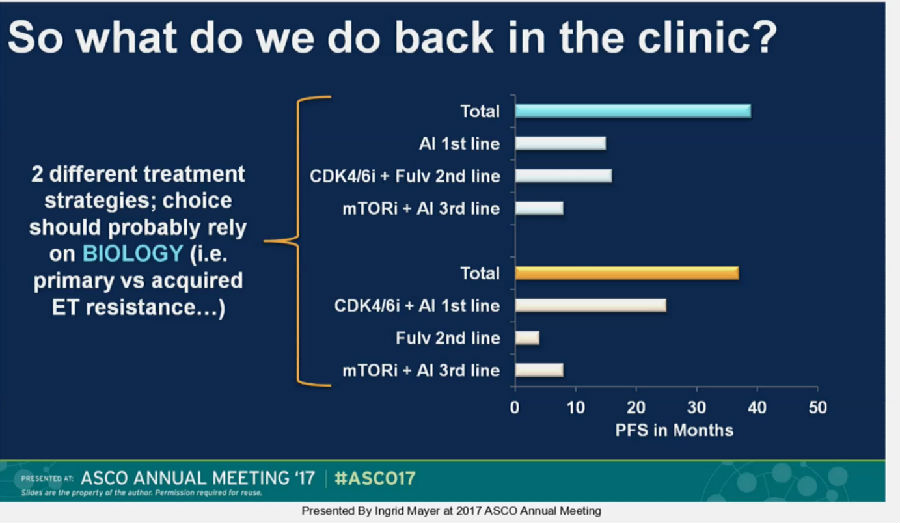
那么,在临床实践中,我们以后将有两种不同的治疗策略可以考虑:
第一种为一线AI,二线CDK4/6抑制剂联合氟维司群,三线mTOR抑制剂联合AI;
第二种为一线CDK4/6抑制剂联合AI,二线氟维司群,三线mTor抑制剂联合AI。
总体来看,这两种策略给患者带来的生存获益相近,这要针对患者的个体情况选择不同的临床治疗策略。
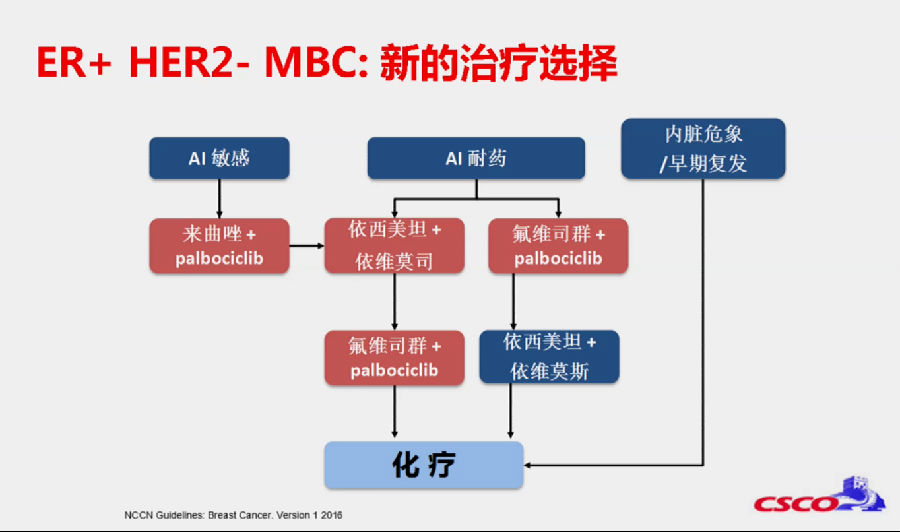
在NCCN指南中现在推荐,如果是AI敏感的患者,可以先选择AI+CDK4/6抑制剂,再尝试依维莫司+依西美坦或氟维司群+CDK4/6抑制剂,进展后应用未选择的二线治疗方案进行三线治疗,而对于一些高危患者也应该考虑到直接应用化疗。
抗Her-2治疗:加法还是减法?
在抗HER-2治疗中,曲妥珠单抗是一个从发现驱动基因,控制驱动基因的经典例子。在曲妥珠单抗1年治疗获得了HER-2阳性乳腺癌辅助治疗“统治地位”后,也不断的受到了很多挑战。
APHINITY研究
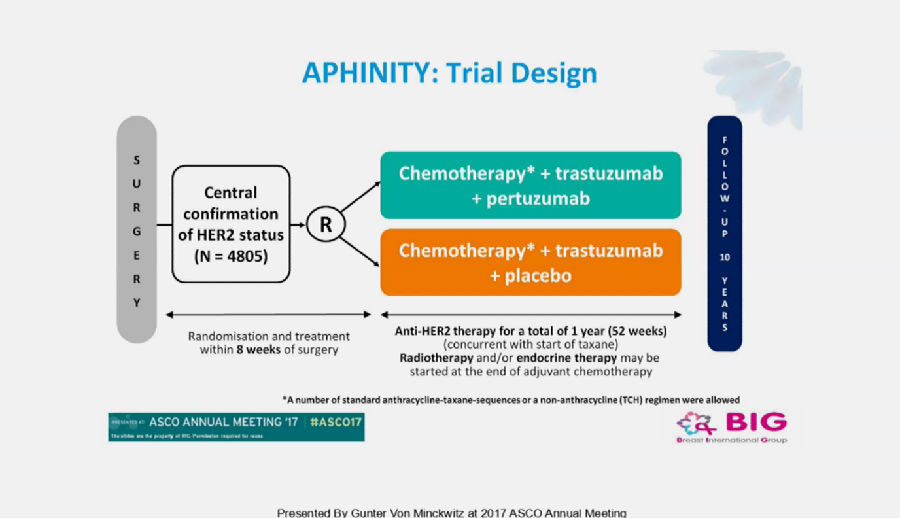
APHINITY研究设计较为巧妙,其目的是探究HER-2阳性乳腺癌的辅助治疗中,在化疗+曲妥珠单抗的基础上,联合或不联合帕妥珠单抗对患者生存结局及安全性的影响。
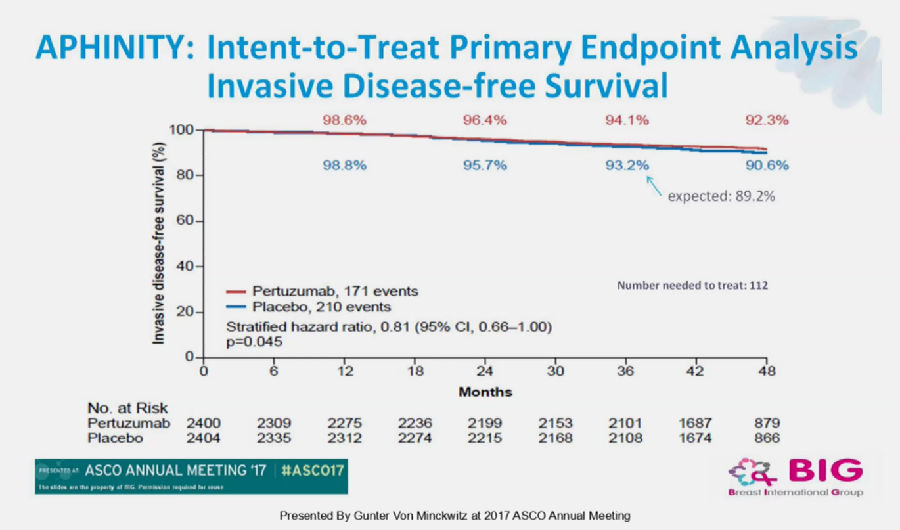
该研究表明,帕妥珠单抗的加入轻微改善了HER-2+乳腺癌患者的无浸润性疾病生存期(iDFS)。两组3年iDFS分别为94.1% vs 93.2%(HR, 0.81; 95%CI: 0.66-1.00; p=0.045)。
对照组的“强大”有些出乎意料(预期对照组3年iDFS为89.2%,实际结果为93.2%)。
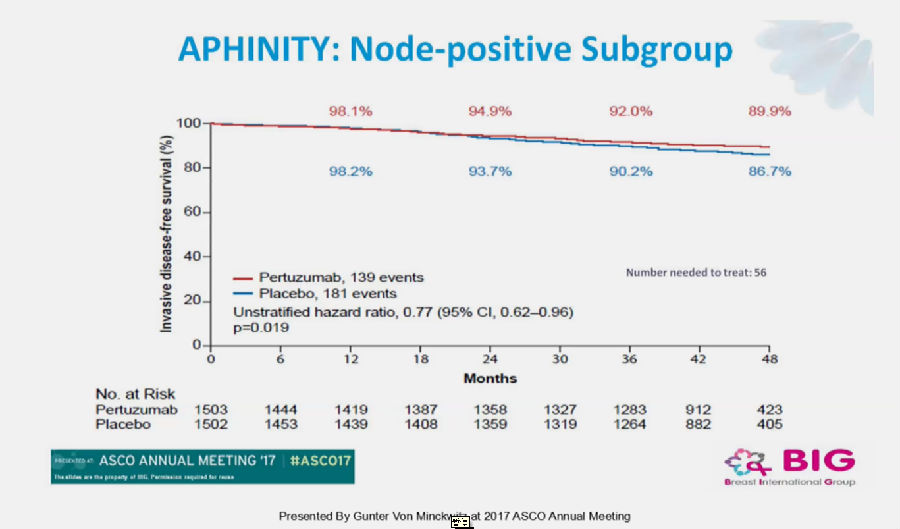
在亚组分析中,对于淋巴结阳性(89.9% vs 86.7%)、激素受体阴性(91.0% vs 88.7%)的患者的4年iDFS改善更为明显。
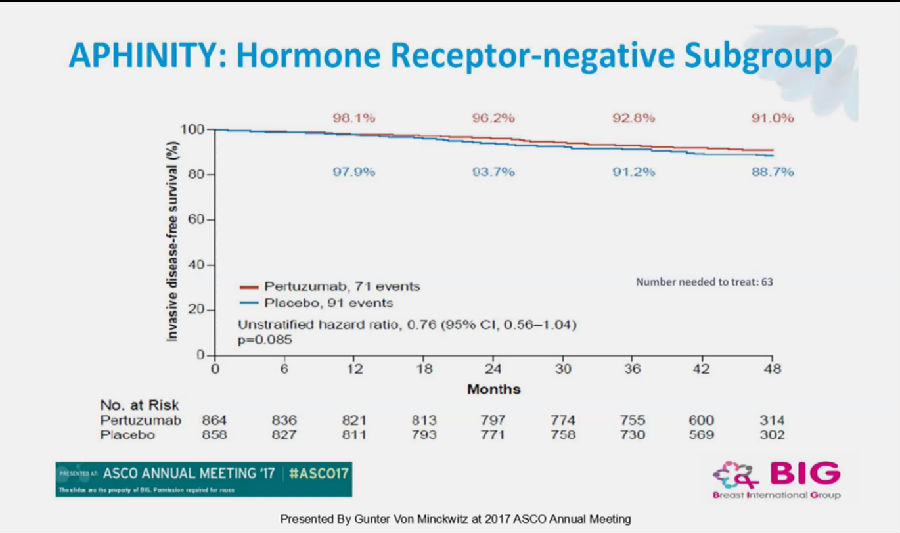
总体来说,APHINITY研究结果达到了主要的研究终点,尚且令人满意。
ALTTO研究
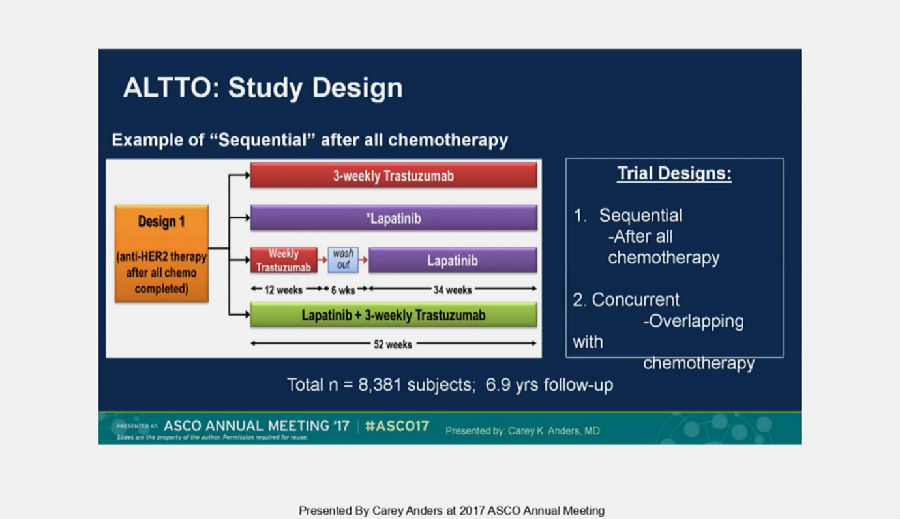
ALTTO研究的设计较APHINITY研究更为复杂,探究拉帕替尼(L)单药,曲妥珠单抗(T)单药,T序贯L和L+T联合方案在HER-2阳性乳腺癌辅助治疗中的疗效与安全性差异。
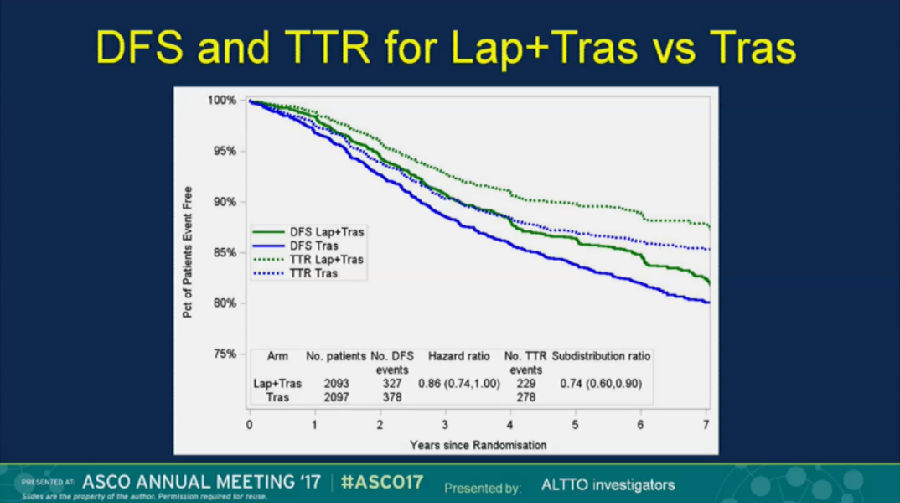
ALTTO研究的未达到优效的主要研究终点,结果不令人满意。但是客观分析来看,如果只对比L+T与T两个亚组,其实联合拉帕替尼产生的获益并不低。

ALTTO研究中,与单药曲妥珠单抗相比,拉帕替尼+曲妥珠单抗也能提高接近3%的6年DFS,对于激素受体阴性的患者的6年IDFS获益率可达4%。
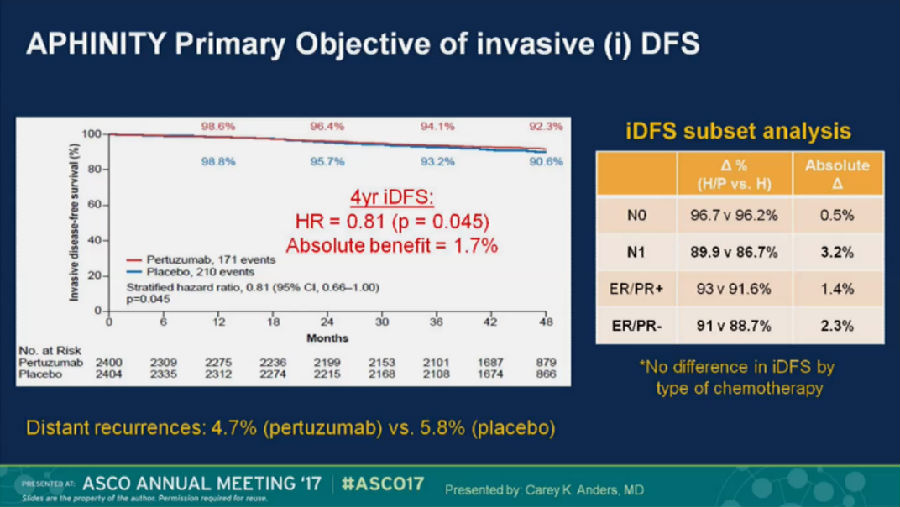
而APHINITY研究带来的4年iDFS获益也只有1.7%,却达到了阳性结果。这可能与实验设计方法有关,这在今后开展临床研究时,是十分值得关注的问题。

缩短抗HER-2治疗疗程的研究也值得关注。虽然Short-HER研究的9周曲妥珠单抗治疗方案没有达到非劣效标准,但是对部分患者来说,缩短抗HER-2疗程可能也是一种选择。
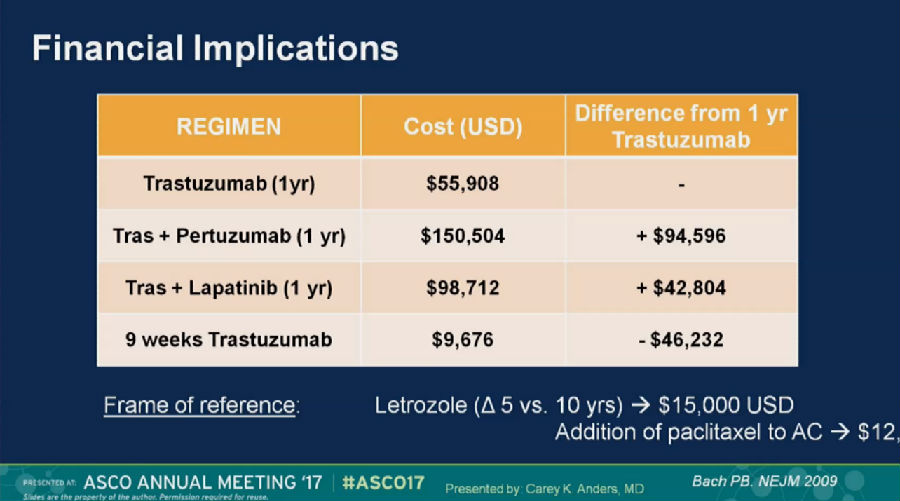
根据美国药物经济学数据,如果行9周单药曲妥珠单抗治疗,只需要花费10,000美金左右。
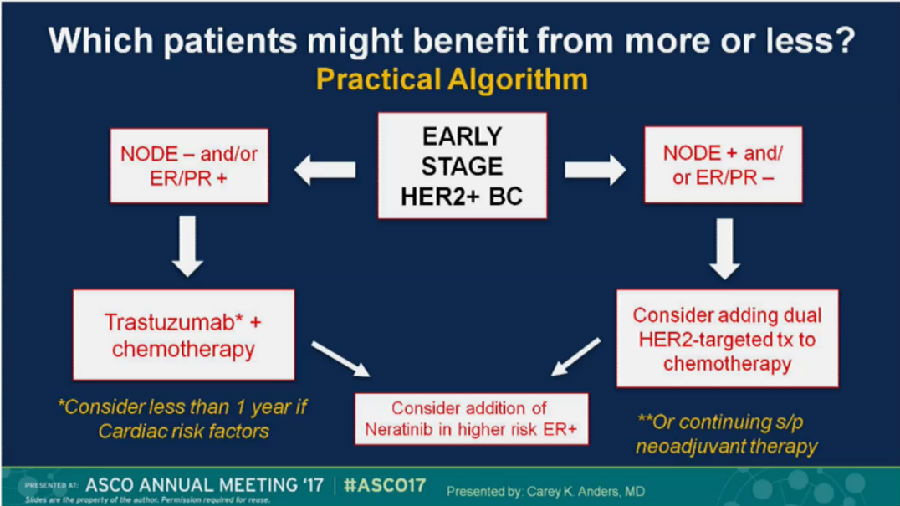
是否在HER-2阳性的患者中,需要根据激素受体状况和淋巴结转移情况进行危险分层,采取不同的治疗方案,也是十分值得深思的问题,需要更多的循证医学证据来证实。
三阴性乳腺癌
对于三阴乳腺癌(TNBC)来说,如果按照临床亚型、内在亚型、免疫情况、突变负荷等进行综合分析,相信可以进一步增大患者改善预后的机会。

在精准医疗的大趋势下,根据TNBC的分子学特征也可能筛选出一些对患者有效的精准治疗药物,提供更多选择。

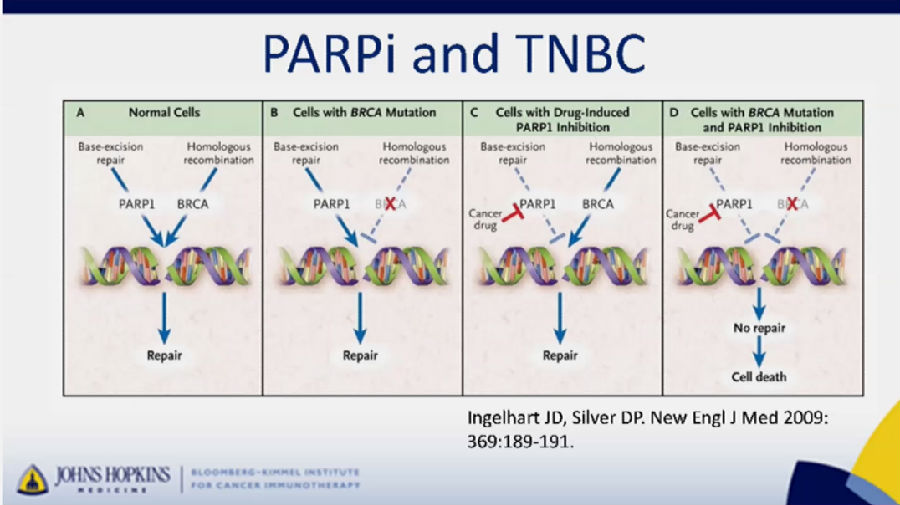
PARP抑制剂
在BRAC突变的TNBC患者中,应用PARP抑制剂进行治疗治疗中也有一定的发展前景。
今年ASCO上汇报的OlympiAD研究,目的探究PARP抑制剂Olaparnib单药对比化疗在BRAC基因突变的,HER-2阴性转移性乳腺癌的疗效与安全性。
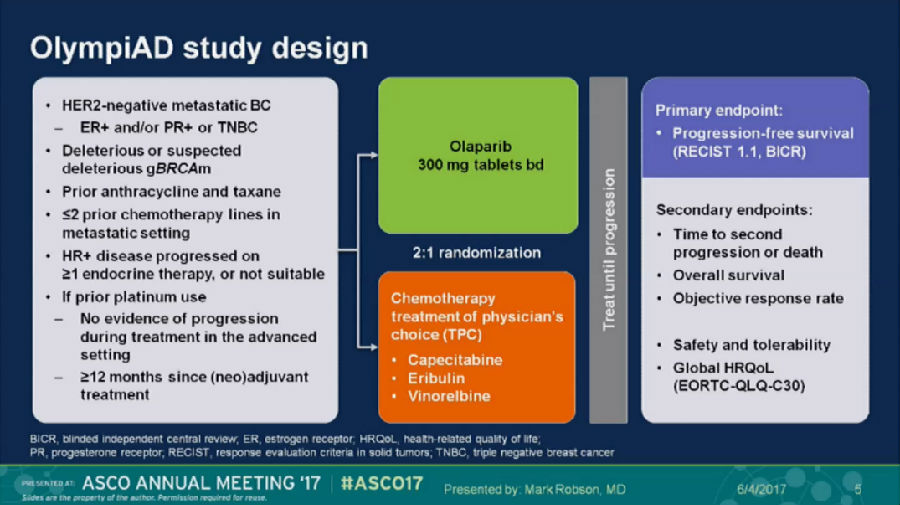
主要研究终点为PFS,次要研究终点为TTP2、OS、ORR、安全性和耐受性、生活质量等。
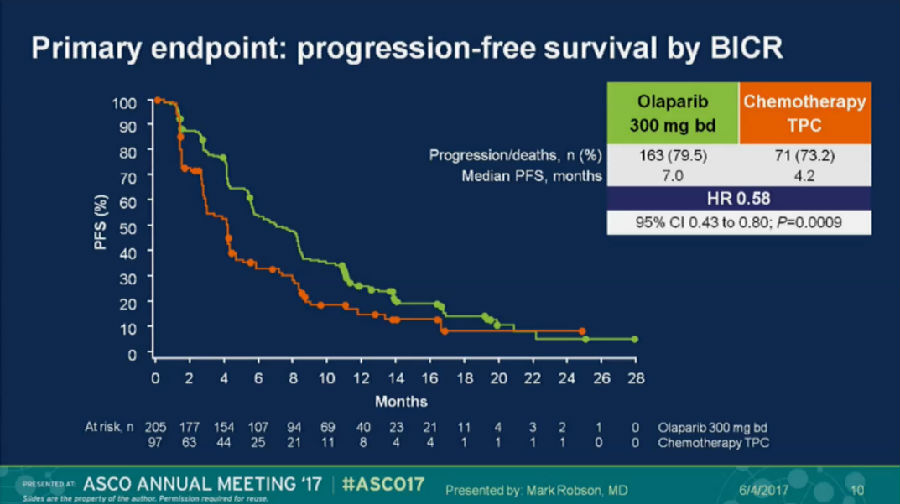
结果表明,Olaparnib与对照组的PFS分别为7.0个月与4.2个月(HR, 0.58; 95%CI: 0.43-0.80; p<0.0009)。
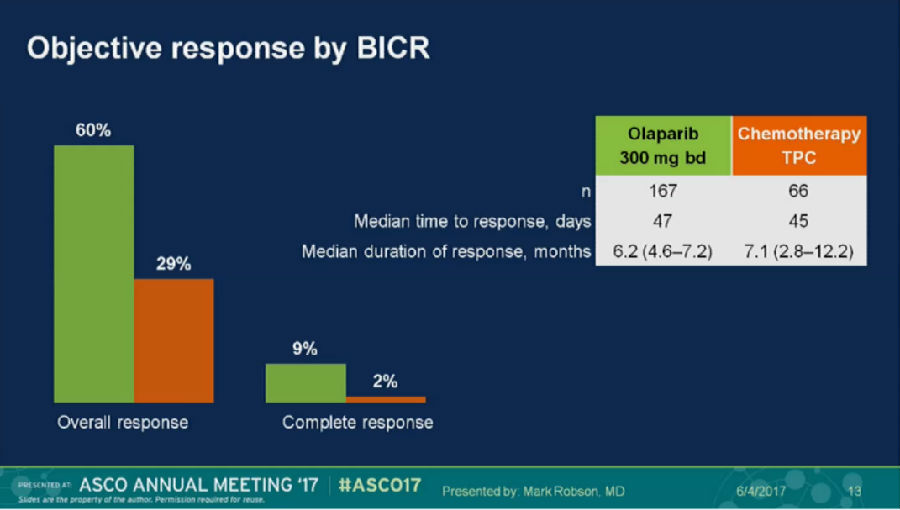
治疗组与对照组的ORR分别为60%和29%,CR率为9%与2%。
但是,患者的BRCA突变概率是较低的,大概只有3%。并且筛选检测的周期也较长,需要3周左右。所以,急需一个更快速的检测方法出炉,尽早筛选出获益人群。
免疫治疗
KEYNOTE-086研究队列A为观察pembrolizumab单药治疗既往接受治疗的mTNBC有效性与安全性的临床研究。

主要研究终点为ORR和安全性,次要研究终点为DOR,DCR,PFS和OS。
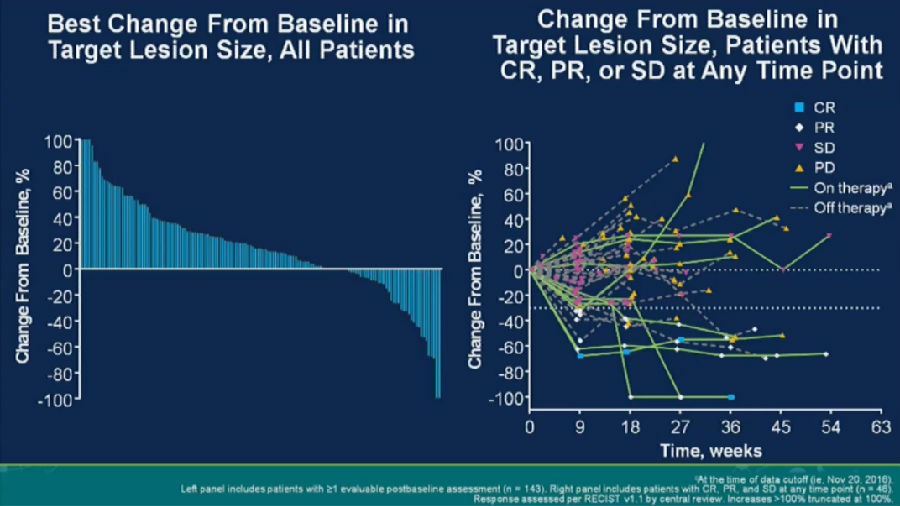
如果未经过PD-L1表达筛选,pembrolizumab单药治疗既往接受治疗的mTNBC,ORR率较低。
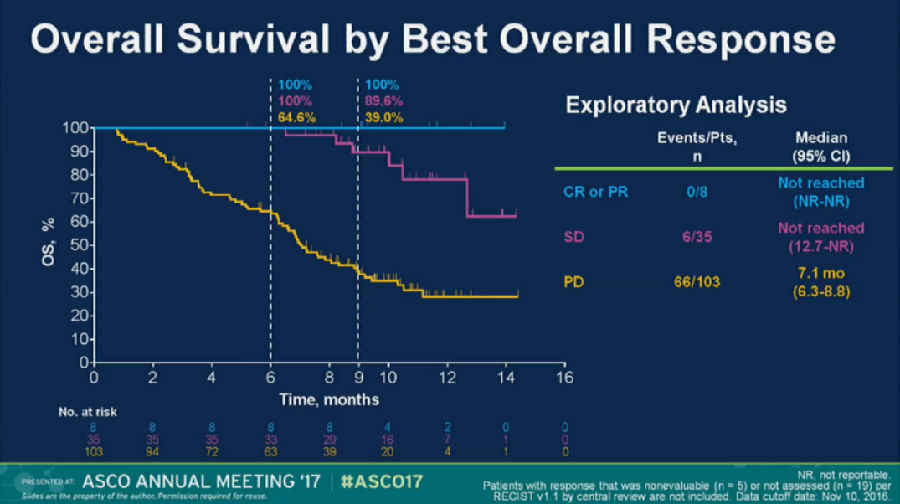
但是,对于有效的患者来说,其生存结局比较令人满意。所以,乳腺癌免疫治疗领域中,我们需要对如何选择更合适的病人,在最合适的时机进行免疫治疗的问题进行进一步的探索。

对于既往接受过多线治疗的患者来说,PD-L1表达与否对疗效影响不大。而对于一线治疗来说,如果患者的PD-L1过表达,那么其有效率也可以达到较高水平。
在乳腺癌新辅助治疗的I-SPY2研究中,免疫治疗联合化疗取得了很好的效果。
所以,我们应该根据Biomarkers筛选患者,并且对未知的Biomarkers进行探索,同时也应对不同治疗阶段进行综合考虑。
CSCO乳腺癌治疗指南
对乳腺癌最新的研究进展解读后,江泽飞教授介绍了CSCO诊疗指南 2017年版的相关内容。

CSCO乳腺癌诊疗指南基于循证医学证据和精准医疗医学的基本原则,基于治疗方法的可及性,制定出最适合我国国情的乳腺癌诊疗指南。

指南分为基本策略和可选策略,对普适性诊治措施和国际上最新进展均有清晰、明确的呈现。

现指南已经发放了20,000余册,并持续加印中。CSCO BC专业委员会致力于乳腺癌规范化诊疗的推广与普及,最近将持续在全国举行CSCO乳腺癌诊疗指南巡讲活动,了解更多乳腺癌诊疗指南内容请关注CSCO BC官方公众号。
